南湖新聞網訊(通訊員 吳小鳳)近期,曹罡教授與(yu) 戴金霞副研究員團隊開發了新型空間組學技術MiP-seq,該技術是基於(yu) 成像的空間多組學雙端原位測序技術(圖1),打破了傳(chuan) 統技術瓶頸,以亞(ya) 細胞、單堿基分辨率同時實現了DNA、RNA、蛋白質和功能小分子的多維空間組學3D圖譜,可以兼容轉錄組、蛋白組、拉曼成像、鈣離子成像多個(ge) 模態信息檢測。該項研究成果以“Spatial multi-omics at subcellular resolution via high-throughput in situ pairwise sequencing”為(wei) 題,於(yu) 5月14日在線發表於(yu) 學術期刊Nature Biomedical Engineering雜誌。
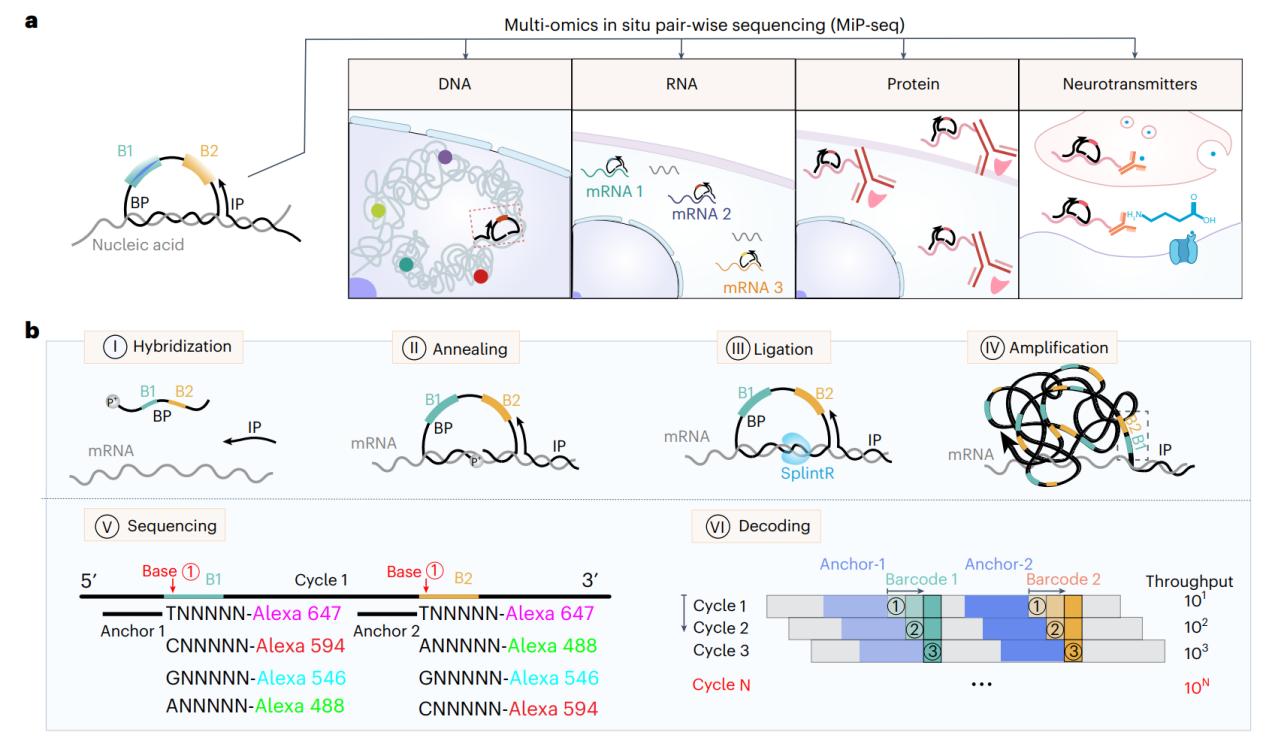
圖1:MiP-seq的操作原理及流程示意圖
解析組織空間異質性及其分子空間表達模式的空間組學是生命科學研究的關(guan) 鍵前沿技術,其多組學拓展廣度與(yu) 高通量檢測深度已為(wei) 各研究領域的熱點問題帶來了新的發現與(yu) 見解。空間組學方法主要分為(wei) 基於(yu) 二代測序(Next generation sequencing, NGS)捕獲或成像策略兩(liang) 類。基於(yu) NGS的空間組學方法可進行全基因組、轉錄組範圍的捕獲,且部分方法可拓展至多組學,但缺乏單細胞分辨率,而且檢測效率較低、成本較高、批間差異較大,重構的空間組學圖像實質為(wei) 2D馬賽克間斷式平麵圖片;基於(yu) 成像的空間組學方法具有亞(ya) 細胞分辨率,且捕獲效率高,部分方法兼容多組學,可利用成像實現3D無間斷空間組學,但大多數方法為(wei) 靶向空間組,全轉錄組模式捕獲效率較低,多輪成像光毒性大,高密度信號解析困難。因此各種空間組學方法都亟待進一步升級,以滿足科研對空間組真正單細胞高分辨、高捕獲率、高重複性的迫切需求。
MiP-seq的主要創新點有五點,一是MiP-seq采用雙條形碼鎖式探針設計和雙端測序策略。與(yu) 傳(chuan) 統的單條形碼鎖式探針和單端測序策略相比,本方法具有更高的解碼能力(10N vs 4N),並且需要的測序輪數顯著減少。因此MiP-seq可以大幅降低測序和成像成本,並且可以節省約50%的成本及測序時間。同時與(yu) 單條碼和單端測序相比,雙條碼測序策略可以顯著縮短成像時間,從(cong) 而最大限度地減少光毒性;二是MiP-seq成功實現了原位多組學檢測(圖2),以亞(ya) 細胞分辨率同時描繪了同一切片中DNA、RNA和蛋白質的空間景觀以及神經遞質的空間分布。這種綜合性的空間多組學方法以往未被報道過;三是光信號擁擠是幾乎所有基於(yu) 成像空間組學方法的“瓶頸”問題。MiP-seq提出了一種序列稀釋策略,通過使用一組測序引物和錨定基因引物來解決(jue) 信號擁擠問題,將極大地促進高密度信號的精確解析;四是與(yu) 當前的原位測序方法相比,MiP-seq的探針設計策略及生化反應體(ti) 係顯著提高了原位測序檢測效率。同時,MiP-seq可以達到單核苷酸分辨率來檢測 DNA 和 RNA 的單堿基突變、單核苷酸多態,並可以區分 RNA m6A 修飾。基於(yu) MiP-seq的高通量和單堿基精度,小鼠海馬中親(qin) 代基因的等位基因空間特異性表達模式得以解析;五是MiP-Seq與(yu) 拉曼成像和活體(ti) Ca2+成像相結合,獲得了具有多維信息的組織圖譜,對解析細胞表達譜與(yu) 功能的關(guan) 聯十分必要(圖3)。
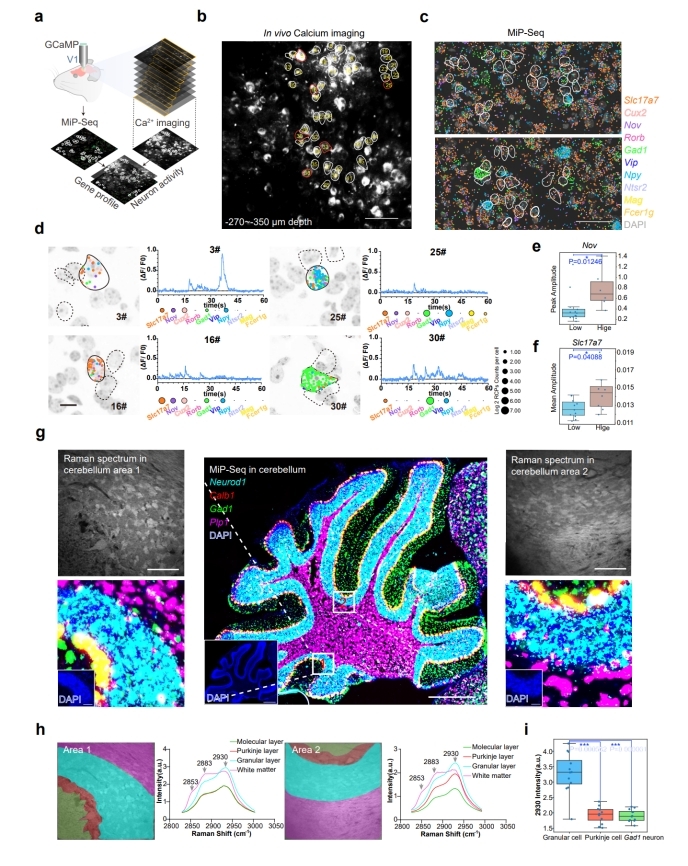
圖2:應用MiP-seq解析彌漫性大B淋巴瘤組織樣本中30種蛋白及6種mRNA的空間分布
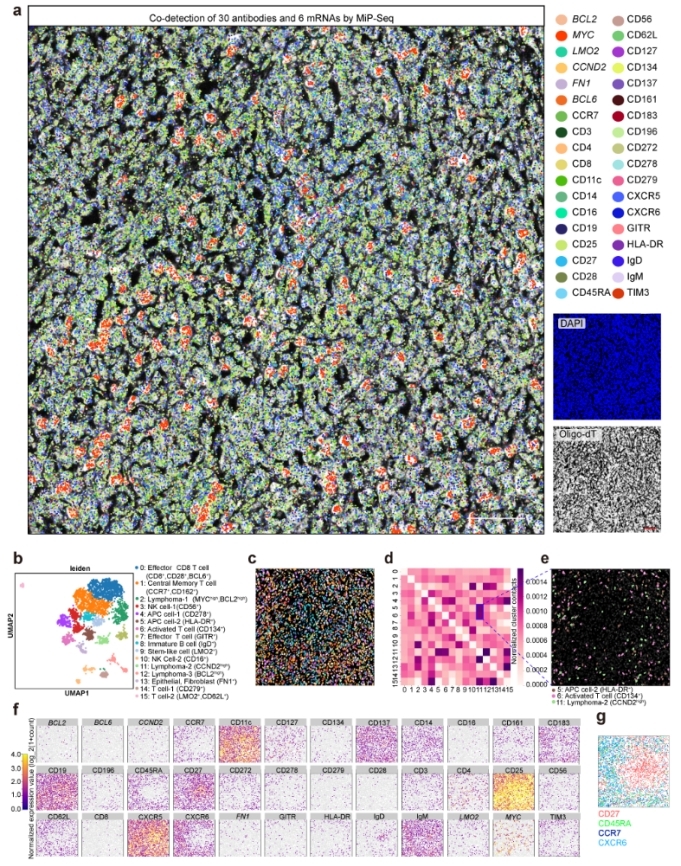
圖3:MiP-seq與(yu) 體(ti) 內(nei) Ca2+成像和拉曼成像整合分析
綜上所述,MiP-seq方法在捕獲策略、解碼通量、靶標檢測範圍、高密度成像、SNV、RNA修飾、功能成像整合分析等方麵進行了優(you) 化與(yu) 提升。相較於(yu) 現行的空間組學方法有其獨特的優(you) 勢,在靶向空間多組學細分領域具有可觀的應用價(jia) 值及前景。這種高檢測效率的空間多組學方法將為(wei) 發育生物學、腦科學、免疫學、腫瘤學、微生物學等領域提供更精準的高空間分辨率的多維空間圖譜。以生物分子的實景還原方式來解析細胞行為(wei) 與(yu) 功能的方式更精準地揭示了生命進程。本技術已實現產(chan) 業(ye) 轉化(鯤羽生物https://www.spatialfish.com/),將為(wei) 基礎科學研究與(yu) 臨(lin) 床分子病理診斷提供高效的空間多組學服務。
據悉,曹罡教授、戴金霞副研究員為(wei) 該論文共同通訊作者,我校吳小鳳博士後和徐偉(wei) 澤博士生為(wei) 該論文的共同第一作者。該工作得到了國家自然科學基金委創新群體(ti) 項目、聯合基金項目和麵上項目的資助。
審核人 戴金霞
原文鏈接:https://www.nature.com/articles/s41551-024-01205-7
【英文摘要】
Technology for spatial multi-omics aids the discovery of new insights into cellular functions and disease mechanisms. Here we report the development and applicability of multi-omics in situ pairwise sequencing (MiP-seq), a method for the simultaneous detection of DNAs, RNAs, proteins and biomolecules at subcellular resolution. Compared with other in situ sequencing methods, MiP-seq enhances decoding capacity and reduces sequencing and imaging costs while maintaining the efficacy of detection of gene mutations, allele-specific expression and RNA modifications. MiP-seq can be integrated with in vivo calcium imaging and Raman imaging, which enabled us to generate a spatial multi-omics atlas of mouse brain tissues and to correlate gene expression with neuronal activity and cellular biochemical fingerprints. We also report a sequential dilution strategy for resolving optically crowded signals during in situ sequencing. High-throughput in situ pairwise sequencing may facilitate the multidimensional analysis of molecular and functional maps of tissues.



